「六年制學程/01/2013.12.10」修訂間的差異
跳至導覽
跳至搜尋
(新頁面: 分類:六年制學程/01 ==元素電子組態== {{模板:元素電子組態}} ===電子式=== #中間寫元素名稱 #元素名稱的上左下右,分別代表外層電子的s...) |
(正在將頁面替換為 '分類:六年制學程/01 {{:化學鍵}}') |
||
| 第1行: | 第1行: | ||
[[分類:六年制學程/01]] | [[分類:六年制學程/01]] | ||
| − | + | {{:化學鍵}} | |
| − | {{ | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
於 2015年7月17日 (五) 01:34 的最新修訂
元素電子組態
| 元素電子組態 | |||||||
| s1 | s2 | ||||||
| 1 氫 1.008 |
2 氦 4.003 |
||||||
| s1 | s2 | p1 | p2 | p3 | p4 | p5 | p6 |
| 3 鋰 6.941 |
4 鈹 9.012 |
5 硼 10.81 |
6 碳 12.01 |
7 氮 14.01 |
8 氧 16.00 |
9 氟 19.00 |
10 氖 20.18 |
11 鈉 22.99 |
12 鎂 24.31 |
13 鋁 26.98 |
14 矽 28.09 |
15 磷 30.97 |
16 硫 32.07 |
17 氯 35.45 |
18 氬 39.95 |
| 19 鉀 39.1 |
20 鈣 40.08 |
||||||
電子式
- 中間寫元素名稱
- 元素名稱的上左下右,分別代表外層電子的s、px、py、pz四個軌域。
- 每個軌域可放0-2個電子,外層 sp 軌域共可放八顆電子,放滿時最穩定。
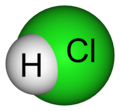
化學鍵(造分子)
參考資料:
分子內
| 離子鍵 | 共價鍵 | 金屬鍵 | |
|---|---|---|---|
| 組成 | 金屬+非金屬 | 非金屬+非金屬 | 金屬+金屬 |
| 作用 方式 |
正負電相吸 | 共用電子對 | 自由電子在相鄰 原子間跑來跑去 |
| 能量 | 150~400 KJ/mole | 150~400 KJ/mole | 50~133 KJ/mole |
| 方向性 | 無 | 有 | 無 |
| 例如 | NaCl、MgO(簡式) | H2、H2O(分子式) | Na(簡式) |
離子鍵
一方失去電子,一方得到電子
共價鍵
共用電子對
- 氫共價鍵
- 氧共價鍵:
- 水的共價鍵:影片 The Chemistry of Water ,字幕翻譯獎學金 200 元。
金屬鍵
- 外層要有很多空軌域。
- 把電子打出軌域的游離能較低。
- 外層要有多餘的電子。
- 電子在相鄰原子的空軌域跑來跑去,叫做「自由電子」。
- 原子浸在自由電子形成的「電子海」中。
影片:Metallic bonding 字幕翻譯獎學金 350 元。
影片:Bonding in Metals 字幕翻譯獎學金 1000 元。
分子間
- 氫鍵:分子極性,正負電相吸。
- 凡得瓦力:電子的機率運動,產生的瞬間偶極矩。
化學反應式

| |
 | 
|
電解水(吸電能)
2H2O→2H2+O2
燃燒氫(放熱能)
2H2O←2H2+O2
合併上兩式:
2H2+O2↔2H2O
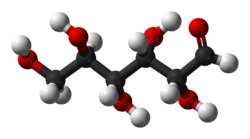
各種分子
負端寫右邊,正端寫左邊